「温故知新」という言葉は、論語の一節「子曰く、故(ふる)きを温(たず)ねて新しきを知れば、以て師たるべし」に由来します。「昔の物事を研究し吟味して、そこから新しい知識や見解を得る(広辞苑)」という意味です。私たちの研究室では、多様で複雑な機能をもつタンパク質(遺伝子)が40億年の間にどのように進化してきたのかを研究することで、その構築原理を学び、その知識を応用して、医療や環境・エネルギー分野に役立つ新しいタンパク質を創り出すことを目指しています。
<タンパク質は生命活動の主役!>
タンパク質は多種多様であり、筋肉だけではなく髪の毛も透明な眼球も体の大部分を異なるタンパク質が構成しています。また、食べ物を消化する酵素も、インスリンなどのホルモンも、匂いや味や光を感知する受容体もすべてタンパク質です。このようにタンパク質は様々な機能を果たしており、生命におけるもっとも基本的な機能性分子と言えます。このタンパク質の実体は、20種類のアミノ酸が数十〜数千個つながった鎖状の分子であり、そのアミノ酸の文字列(配列)に応じて固有の形に折れたたみ、固有の機能を発揮します。多種多様なタンパク質ができる理由は、アミノ酸配列の違いに起因しており、その配列情報は
ゲノム
のDNAに保存されています。DNAは4つの塩基(A,C,G,T)からなる文字列ですので、それを20文字のアミノ酸配列に変換するために、すべての生命は、連続する3つの塩基を1つのアミノ酸に対応させて暗号化しています(例えば、GGGはグリシン、GAGはグルタミン酸という具合に)。現代の遺伝子工学の一般的な技術を使えば、好きな配列をもつ人工遺伝子を合成して、その情報を元に人工タンパク質を作ることは簡単にできます。しかし、どのような配列をデザインすれば、欲しい機能をもつタンパク質ができるかを予測することは簡単ではありません。そこで私たちは、現存する高性能なタンパク質がどのように進化してきたのかを探り、それを実験室内で再現できれば、新しいタンパク質を創ることができるのではないかと考えました。
では、タンパク質の進化はどのようなメカニズムで起こるのでしょうか? 上で述べたように、タンパク質のアミノ酸配列はDNAの塩基配列に暗号化されています。そのDNAがコピーされ、遺伝子として、子孫に受け継がれます。このコピーが100%完全であればすべての生命は全く同じ遺伝子をもつクローンとなり、進化は起こりません。しかし、実際にはDNAの文字列をコピーするときに頻度は低いですがランダムなエラー(変異)が生じ、それによって遺伝子の文字列が書き換えられます(例えば、ある遺伝子の塩基配列の1文字がGからAに変化すると、それに対応するタンパク質のアミノ酸配列の1文字がグリシンからグルタミン酸に変化するという具合に)。このアミノ酸の変化によってタンパク質の機能が失われてしまった場合、もしその機能が生存に必須であれば、その変異をもつ個体は生存できず子孫を残せないので、そのような「不利な変異」は淘汰されます。一方、このアミノ酸の変化によってタンパク質の機能が向上し、その変異をもつ個体の生存にとって有利に作用した場合、そのような「有利な変異」は代々子孫に受け継がれて集団中に広まっていきます。こうしてランダムな「変異」と機能の「選抜」を繰り返すことによって、低い機能をもつ文字列から次第に高い機能をもつ文字列に「進化」していくという現象が起こります。
<タンパク質の実験室内進化>
この「変異」と「選抜」を繰り返す進化の原理を利用して、実際に実験室でタンパク質を進化させるためには、さまざまな工夫が必要となります。例として、ある標的分子に結合するタンパク質を人為的に進化させて結合力を向上させるケースを考えましょう(図1)。まず、PCRという手法を用いて、そのタンパク質の遺伝子に変異を入れつつ増幅し、多様な変異をもつ集団(ライブラリー)を作ります(図1①)。次に、この遺伝子の集団をタンパク質の集団に生物学的に変換します(図1②)。このとき、私たちのオリジナルな技術を使って、タンパク質とその遺伝子を物理的に連結しておくのがポイントです。最後に、あらかじめ標的分子を固定しておいたカラムを使って、標的分子に強く結合するタンパク質のみを選抜した後(図1③)、連結しておいた遺伝子を回収します(図1④)。回収したDNAの塩基配列は自動シークエンサーにより容易に解読することができます。この遺伝子を元にしてさらに変異を導入し、この進化サイクルを繰り返します。サイクルが進むに連れて「選抜」の条件を過酷にしていくことで、次第に結合力の高いタンパク質に進化させることができます。
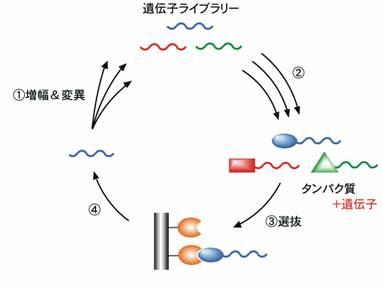
私たちが生命の進化から学ぶのは、おもに、最初にどのような変異ライブラリーを作成すれば、高い機能をもつタンパク質を得る確率が高くなるかという点です。例えば、生物は遺伝子をシャッフルすることで「有利な変異」を効率よく組み合わせて進化スピードをアップしたり、有利でも不利でもない「中立な変異」を蓄積しておくことで環境が変化したときに新しい機能を生み出したりしていることが分かってきました。実際に、このような仕組みを実験系に取り入れると、実験室内でもタンパク質が進化しやすくなることが証明されつつあります。
すでに、これまでに世界中で多くのタンパク質が実験室内進化によって改良されています。例えば、2008年のノーベル化学賞で話題になったオワンクラゲの緑色蛍光タンパク質は、人為的な変異により青色や黄色など様々な色の蛍光タンパク質に進化させることでその応用価値が高まり、 細胞を「見える化」する技術 などに広く利用されるようになりました。
最後に、私たちの研究室で進行中の応用研究をいくつか紹介しましょう。
<医療分野への応用:バイオ医薬>
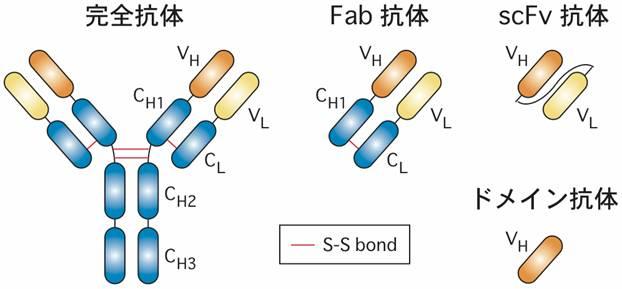
従来の化学合成技術を利用した低分子医薬に対して、タンパク質や遺伝子などを利用した医薬品をバイオ医薬といいます。その代表格が抗体医薬です。抗体とは、私たちの体内に侵入した細菌やウイルスなどの異物を認識して結合し、攻撃・排除するタンパク質ですが、この抗体の性質を利用して、がん細胞やリウマチの原因分子を識別して攻撃するのが抗体医薬です(図2)。バイオ医薬は元々生体の中にある分子なので副作用の心配が少ないなどの利点があり、近年多くのバイオ医薬が開発されています。しかし、細胞を培養してタンパク質をつくらせる必要があるため、化学合成と比べて薬の費用が高くなってしまうという欠点があります。私たちの研究室では、試験管の中でタンパク質を高速に進化させるオリジナルな技術を確立し、がんやウイルス感染に対する抗体医薬の結合力を強化することで薬効を向上させたり、図2右側に示すように抗体を断片化して小さくすることで大量生産しやすくする研究をおこなっています。このような手法を確立することで、将来的には様々な抗体医薬を改良して、それらの投薬量を減らしたり、生産コストを下げることが期待できます。
<環境・エネルギー分野への応用:バイオマスとバイオ電池>
バイオマスとは、元々「生物資源量」という意味の生態学用語ですが、近年は再生可能なエネルギーとなり得る生物資源として注目されています。特に、食料と競合しない木質廃材や稲藁などのセルロース系原料の有効利用に期待がもたれています。セルロースはブドウ糖が鎖状につながったものであり、セルロース分解酵素というタンパク質によりブドウ糖にまで分解できれば、その後、発酵によりバイオエタノールを作ったり、後述するように直接電気に変換することが可能となります。私たちの研究室では、セルロース分解酵素を実験室内で進化させることで、従来よりもセルロース分解活性の高い人工酵素を創り出す研究をおこなっています。
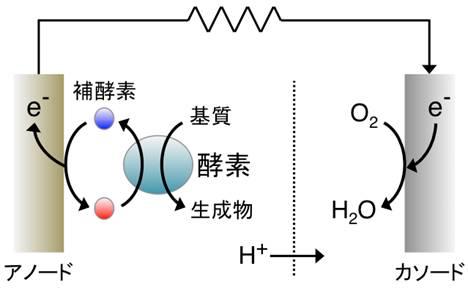
一方、バイオ電池は、酸化還元酵素(これもタンパク質です)を利用して有機物(ブドウ糖などの基質)を分解し直接電気に変換できる未来のエネルギーデバイスとして期待されています(図3)。ドラえもんがドラ焼きを食べて(今なら、フランキーがコーラを飲んで?)動くことができるのも、おそらくバイオ電池を搭載しているからでしょう。しかし、現段階のバイオ電池は出力や寿命に限界があり、実用化には至っていません。私たちの研究室ではロボットは作れませんが、酸化還元酵素の活性や安定性を高めることでバイオ電池の出力や寿命を向上できるのではないかと考え、学内外の研究室と共同して酸化還元酵素の進化実験系を構築しています。
<面白いことは役に立つ!>
生命の進化の歴史を研究することは、究極的には私たちがどこから来たのかを問うことでもあり、それ自体が大変「面白い」テーマですが、「面白い」ことは「役に立つ」というのも科学の歴史が示す経験則です。150年以上前、電磁気学の祖であるファラデーの簡単な電気実験を見た貴婦人が「とても面白いですが、それは何の役に立つのですか?」と尋ねたのに対して、ファラデーが「生まれたばかりの赤ん坊が役に立ちますか?」と答えたというのは有名な話です。現代の私たちの生活にとって電気がなくてはならないものであることは、昨年の震災後にあらためて痛感したばかりです。過去のタンパク質(遺伝子)の進化の「面白い」仕組みを研究することで、バイオ医薬やバイオ電池に「役立つ」新しいタンパク質を創り出し、人類の抱える問題の解決に微力ながら貢献していきたいと考えています。


