自然界に広く存在し、私たちの体内にも見られる複合脂質は、長い間、細胞膜の一部として機能すると考えられてきました。しかし、最近の研究で、複合脂質が膜構成成分としてだけでなく、“シグナル伝達分子”としても重要な役割を担っていることが明らかになってきました。具体的には、免疫の働きを調節する等、体内の重要な機能に関与しています。しかし、自然界の複合脂質は似たような構造を持つ分子が多様に混在していることが多く、単一分子としての複合脂質の機能の詳細を理解するのは困難でした。
一方、自然免疫は、免疫細胞に存在する“受容体”タンパク質が特定の分子を検出するセンサーとして機能することで駆動します。さらに自然免疫は、複数の受容体が協働的かつ複雑に作用することで、免疫応答を精密に制御していると考えられています。その中でも、複合脂質を認識し、自然免疫応答を調節する受容体として、Toll-like receptors(TLRs)やC-type lectin receptors(CLRs)等が知られていますが、これらの自然免疫受容体に対して複合脂質が関与する制御メカニズムには、まだ解明されていない点が多く残っています。
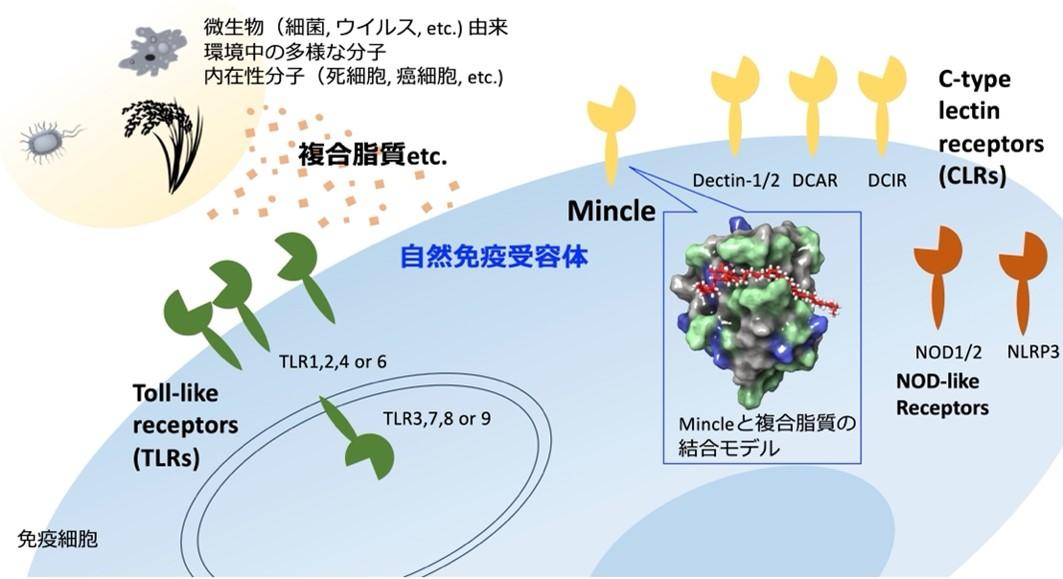
図1 複合脂質と自然免疫受容体の概要図
こうした背景を踏まえ、私たちは、複合脂質による免疫調節の仕組みを明らかにすること目指して研究を行っています。そのアプローチとして、まず単一分子としての複合脂質を得るため、化学合成によって複合脂質を効率的に得る合成法を確立します。確立した手法を用いて、種々の誘導体を合成した後、免疫活性化能を評価し、脂質構造と免疫活性化の相関を明らかにします。また計算化学や物理化学解析、あるいは分子プローブ創製を活用した種々の免疫機構解析を用いて、複合脂質あるいは自然免疫受容体の機能を明らかにします。
一例として、CLRの一種であるMincleに関連した研究を紹介します。Mincleは結核菌由来のトレハロースジミコール酸(TDM)をはじめとする天然由来複合脂質や自己糖脂質を認識し、自然免疫を活性化することが報告されています。しかし、リガンドの脂肪酸部位とMincleの相互作用の詳細は明らかになっていませんでした。
私達はMincleとリガンドの結合モデルを基に、トレハロースジエステルの脂肪酸部位に極性基を導入した脂質改変誘導体を化学合成し、活性評価へと展開したところ、脂肪酸部位にヒドロキシ基(OH基)を導入した誘導体が活性を保持する結果を得ました。さらに結合シミュレーション解析を行ったところ、リガンド脂肪酸部位のOH基がMincle表層付近のアスパラギン酸(Asp)と水素結合を形成する可能性が示唆され、この相互作用が誘導体の活性保持に寄与したと考えています。このように、本研究ではMincleリガンドの分子設計において重要となる新たな指針を構築しました。また、この成果はMincleとリガンドの相互作用を分子レベルで理解し、免疫活性化に関する研究をさらに発展させる基盤となります。
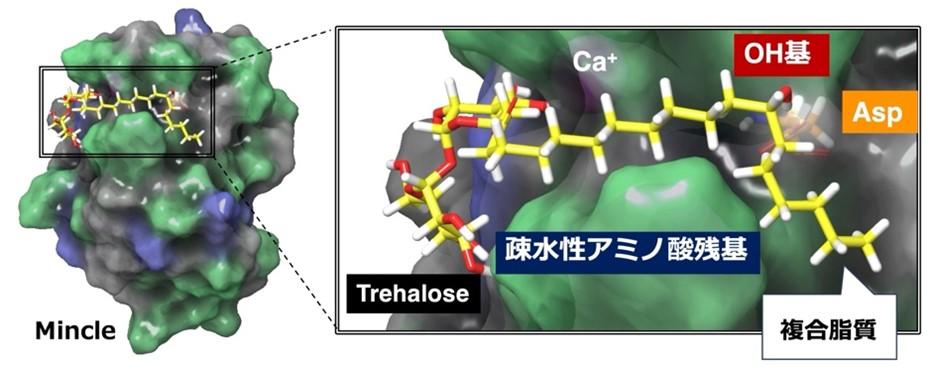
図2 Mincleと複合脂質の結合様式解析
免疫機構は非常に複雑な仕組みではあり、未だ解明されていない部分が数多く存在します。しかし、本研究のように有機合成化学をはじめとする様々な知識や技術を使った学際的なアプローチによって解析することで、従来の方法では見えなかった新たな知見を得ることが可能です。このような学際的なアプローチが研究の面白さであるとともに、未知の領域に挑戦し、新たな発見を楽しむことが科学研究の醍醐味だと感じています。これからもさらなる発見を目指し、研究を展開していきたいと考えています。



